Chemie-Wissen / Radon

Radon – Element im PSE
Radon ist ein chemisches Element im Periodensystem der Elemente (PSE) mit der Ordnungszahl 86 und dem Elementsymbol Rn. Das chemische Element ist in der 6. Reihe (Periode) im Block p (p-Orbital) im PSE zu finden.
Wie beispielsweise Argon, Neon und Xenon wird Radon der 18. Elementgruppe, den sogenannten Edelgasen, zugeordnet.
Eigenschaften von Radon
Radon ist ein natürlich vorkommendes, radioaktives Gas, welches unter Normalbedingungen farblos, geruchlos und geschmacklos ist. Die Siedetemperatur von Radon beträgt -61,8 °C, während die Schmelztemperatur -71 °C beträgt. Mit einer Dichte von 9,73 mg/cm³ ist Radon das schwerste aller elementaren Gase. Diese hohe Dichte sorgt dafür, dass sich das Gas in physiologisch bedeutenden Mengen, besonders in Kellern und den unteren Stockwerken, in Gebäuden ansammeln kann.
Da Radon ein Edelgas mit einer abgeschlossenen Elektronenschale (hohe chemische Stabilität) ist, ist es chemisch fast nicht reaktiv, auch nicht mit seiner Umwelt, der Luft, dem Wasser oder dem Boden. Es reagiert lediglich mit Fluor zu Radonfluorid. Dabei verhält es sich ähnlich wie Xenon, wobei Radon-Verbindungen deutlich stabiler sind. Trotzdem stellt das Studium der Radon-Chemie eine große Herausforderung dar, was unter anderem mit der hohen spezifischen Aktivität des Elements zusammenhängt, die dazu führt, dass energiereiche Strahlung eine Selbstzersetzung (Autoradiolyse) der Verbindungen bewirkt.
Radon Isotope
Insgesamt sind 36 Radon Isotope bekannt (Radon-229 bis Radon-193), welche alle als radioaktiv gelten. Von diesen Isotopen werden nur drei unter natürlichen Bedingungen gebildet:
- Radon-222: Dieses Isotop entsteht innerhalb der Uran-238-Zerfallsreihe durch Alphazerfall von Radium-226 und hat eine Halbwertzeit von 3,82 Tagen. Damit ist es das langlebigste und stabilste natürlich vorkommende Radon Isotop, wodurch es häufig als Tracer in geologischen und biochemischen Untersuchungen genutzt wird.
- Radon-220 (auch: Thoron): Innerhalb der Thorium-232-Zerfallsreihe entsteht bei dem Zerfall des Mutternuklides Thorium-232 das Radon Isotop Thoron mit einer Halbwertzeit von 55,6 Sekunden.
- Radon-219 (Actinon): Innerhalb der Uran-235-Zerfallsreihe (Uran-Actinium-Reihe) entsteht durch Alphazerfall das Isotop Radon-219 bzw. Actinon, welches eine Halbwertzeit von 55,6 Sekunden aufweist.
Radon – Wo kommt es vor?
Radon kommt natürlich und nahezu überall in unserer Umwelt vor, da es unter anderem durch den Zerfall von Uran entsteht, welches in vielen Gesteinen der Erdkruste enthalten ist. Zudem trägt Radon maßgeblich zur natürlichen Strahlenbelastung des Menschen bei. Nach dem Bundesamt für Strahlenschutz beträgt die durchschnittliche jährliche Dosis an Strahlung durch das Gas ungefähr 1,1 Millisievert. Mit diesem Anteil macht Radonstrahlung mehr als 50 % der gesamten natürlichen Strahlenbelastung aus.
Radon in Böden / Gesteinen
In Böden und Gesteinen, welche Uran und Thorium enthalten, wird kontinuierlich Radon gebildet. Dennoch gelten alle Böden und Gesteine als potenzielle Radon-Quelle, wobei die Intensität, abhängig von Gesteinsart und Standort, variieren kann. Viel Radon enthalten zum Beispiel alte magmatische Gesteine wie Granite oder Rhyolithe. Bezogen auf regionale Faktoren enthalten besonders Mittelgebirge aus Granitgestein in Deutschland (z. B. Schwarzwald, Bayerischer Wald, Fichtelgebirge und Erzgebirge) eine besonders hohe Radonkonzentration, wobei der Süden insgesamt mehr Radon aufweist als der Norden von Deutschland.
Radon in der Luft
Radonatome gelangen über den Boden an die Erdoberfläche und werden von dort aus an die bodennahen Luftschichten abgegeben und verteilt. Durch eine schnelle Verteilung kommt Radon in der freien Atmosphäre jedoch nur in sehr geringer Konzentration vor, nämlich lediglich etwa ein Radonatom auf 10²¹ Luftmoleküle, woraus sich eine Strahlenbelastung für den Menschen von 0,1 Millisievert pro Jahr ergibt.
Radon in Wohnräumen
Durch die Radon-Konzentration im Boden und in der Luft kann das Gas durch undichte Stellen aus dem Untergrund in Gebäude eindringen oder sich in Innenräumen sammeln, welche schlecht belüftet sind. In diesem Fall kann Radon sogar ein Gesundheitsrisiko darstellen. Nach dem Bundesamt für Strahlenschutz beträgt die Konzentration in deutschen Wohnräumen ungefähr 65 Becquerel pro Kubikmeter. Dabei ist die Stärke der Belastung abhängig von:
- Radonmenge im Untergrund
- Gasdurchlässigkeit des Bodens
- Dichtheit der Gebäudehülle
- Radongehalt in Baumaterialien und Trinkwasser
- Luftwechselrate der Innenräume
- Lage der Räume innerhalb des Gebäudes (z. B. Kellerräume)
Eine zuverlässige Aussage der Radon-Konzentration eines Wohnraumes kann jedoch ausschließlich durch eine gezielte Radonmessung getroffen werden.
Radon im Wasser
Da Radon wasserlöslich ist, kann es nicht nur durch den Boden oder die Luft, sondern auch über Trinkwasserleitungen in Gebäude gelangen und beim Kochen oder Duschen freigesetzt und eingeatmet werden. Eine Empfehlung der Strahlenschutzkommission besagt, dass die Radon-Konzentration im Trinkwasser unter 100 Becquerel pro Liter gehalten werden sollte, weshalb in Deutschland umfangreiche Messungen durchgeführt wurden. Diese ergaben, dass Regen- sowie Oberflächenwasser deutlich weniger Radon enthalten als Grundwasser, was auf die erhöhte Konzentration des Gases im Boden und in Gesteinen zurückzuführen ist. Dadurch kann ein erhöhter Radongehalt im Grundwasser ein Indikator für eine Grundwassereinspeisung sein.
Radonhaltigen Gewässern wird jedoch auch eine heilende Wirkung zugeschrieben, was auf eine lange Tradition zurückgeht und weshalb diese Quellen häufig Bestandteil von Kurorten sind. Radonhaltige Quellen findet man beispielsweise in Bad Gastein (Gasteiner Heilstollen), Meran, Sibyllenbad, Menzenschwand, Bad Schlema, Bad Kreuznach, Bad Zell und Ischia (Italien).
Weiteres Vorkommen von Radon
- In Baumaterialien, wenn diese aus natürlichem Gestein mit Uran- und Radiumanteilen bestehen
- In Lebensmitteln durch die natürliche Strahlenbelastung
- In Bergwerken: Beim Abbau von Uranerz, Flussspat und Blei
- Industrieanlagen: Labore und Fabriken, in denen Uran, Radium oder Thorium verarbeitet wird
- Höhlen und Rohrleitungen, in welche Radon aus dem Boden diffundiert
Radon – Entdeckung
Radon wurde im Jahr 1900 von Friedrich Ernst Dorn bei Untersuchungen der Zerfallsprodukte von Radium entdeckt. Bei diesen entdeckte er ein schweres Gas, welches er anhand von Mendelejews Periodensystem folgerichtig als Edelgas erkannte, das unterhalb von Xenon steht.
1908 gelang es dann William Ramsay, welcher abgesehen von Helium die restlichen Edelgase des Periodensystems entdeckte, gemeinsam mit dem Engländer Robert Whytlaw-Gray, die Isolierung des zuvor entdeckten Gases durch eine wochenlange Aufkonzentration der Spaltprodukte von Radium. So konnten sie die exakte Masse des Gases bestimmen, welches sie zunächst „Niton“ nannten.
Erst im Jahr 1923 wurde der offizielle Name „Radon“ in Anlehnung an den Namen des Elementes Radium bestätigt.
Radon im Periodensystem der Elemente
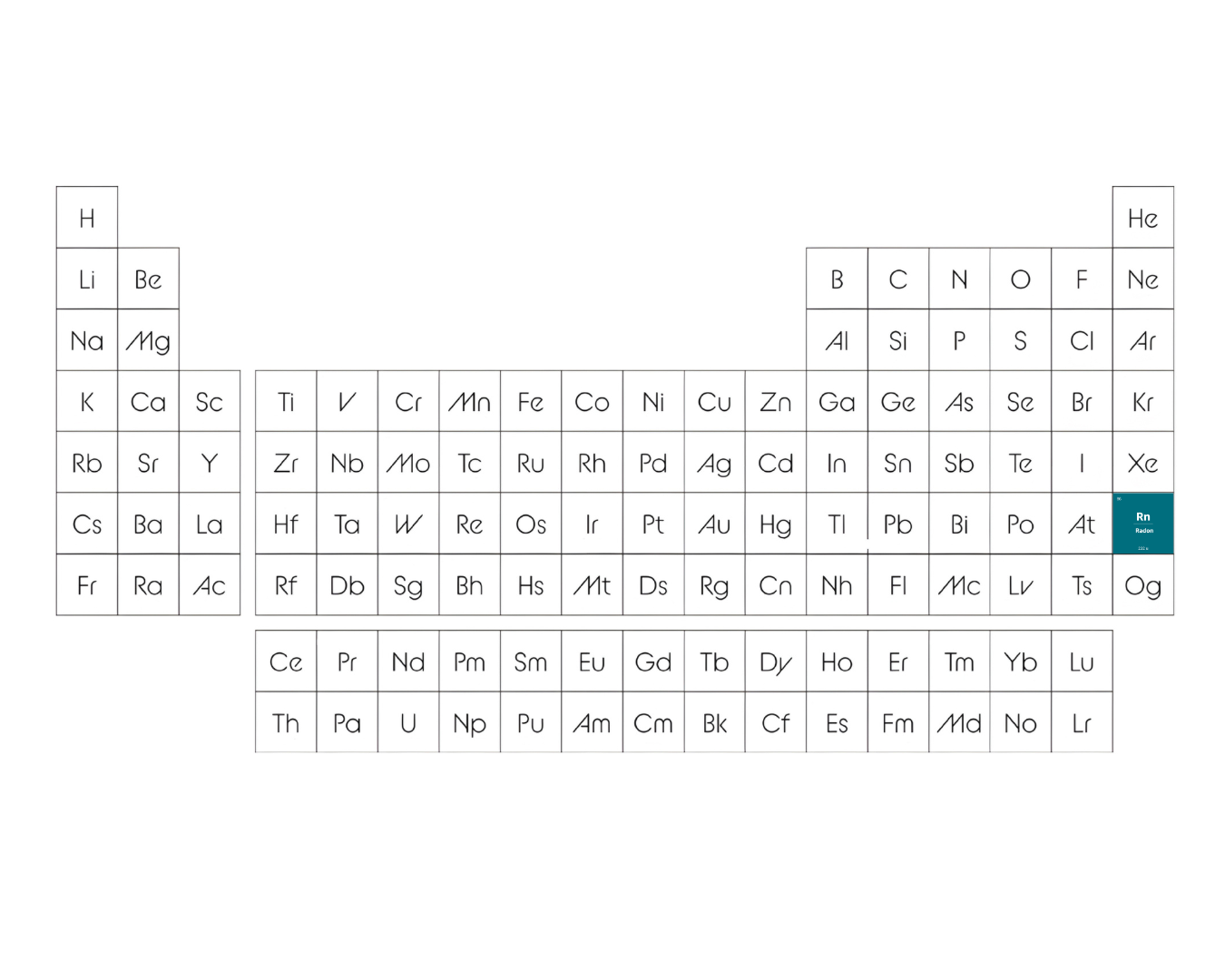
Radon – Verwendung
Aufgrund seiner Radioaktivität und der geringen Halbwertzeit von Radon findet das Gas nur in einigen sehr spezifischen Gebieten Anwendung:
Medizinische Anwendungen von Radon
Radon wird in der medizinischen Balneologie verwendet, um bestimmte chronische Krankheiten, zum Beispiel rheumatische Beschwerden oder Arthrose, zu behandeln, da dem Gas eine angebliche heilende Wirkung zugesprochen wird, welche jedoch nicht naturwissenschaftlich bewiesen ist. Je nach Therapieform erfolgt die Behandlung in Radon-Heilstollen, Heilbädern oder Radon-Dunst- und Luftbädern. Auch Radon-Trinkkuren werden für Behandlungen eingesetzt.
Radon in der Hydrologie
In der Hydrologie kann Radon genutzt werden, um Aufschluss über die Grundwasserversorgung zu geben. Da Regen- sowie Oberflächenwasser nahezu radonfrei sind, kann ein erhöhter Radongehalt im Oberflächenwasser ein Indikator für den Einfluss von Grundwasser sein.
Radonmessungen als Erdebenvorhersage
Da leichte Erschütterungen in der Erde dafür sorgen, dass sich Radongas schneller ausbreitet, steigt die Konzentration des Gases in unterirdischen Hohlräumen messbar an. Daher werden Radonmessungen in vielen Ländern als Indikator für bevorstehende Erdbeben genutzt.
Radon als Indikator für Uranerz-Lagerstätten
Radonmessungen können genutzt werden, um Uranlagerstätten zu identifizieren, da die Menge des aus dem Boden austretenden Radongases maßgeblich vom Radiumgehalt und der Porosität des Untergrundes abhängt. Somit weisen erhöhte Radonwerte auf eine höhere Konzentration von Uran bzw. Radium sowie auf eine gesteigerte Durchlässigkeit des Bodens hin, was ein Zeichen für das Vorhandensein einer Uran-Lagerstätte darstellt. Im Rahmen der Uranprospektion kommen daher häufig einfache, passiv arbeitende Messgeräte zum Einsatz, die großflächig an oder knapp unter der Erdoberfläche ausgelegt werden. Allerdings ist zu beachten, dass geologische Prozesse Uran vom entstandenen Radium trennen können. Daher liefert ein hoher Gehalt an Radon allein keinen eindeutigen Nachweis für Uranvorkommen.
Unsere Quellen - Hier erfahrt ihr noch mehr zu Radon:
Chemie-Wissen von A bis Z
- Aluminium
- Ammoniak
- Antimon
- Argon
- Arsen
- Bakelit
- Barium
- Beryllium
- Bismut
- Blei
- Bor
- Brom
- Cadmium
- Caesium
- Calcium
- Californium
- Chlor
- Chrom
- Cobalt
- Darmstadtium
- Edelmetalle
- Eisen
- Europium
- Erdöl
- Fluor
- Francium
- Gallium
- Germanium
- Glycerin
- Gold
- Haber-Bosch-Verfahren
- Hafnium
- Holmium
- Ionisierungsenergie
- Ionisierungsenergie
-Tabelle - Indium
- Iridium
- Jod
- Kalium
- Katalysator
- Kohlenstoff
- Krypton
- Kupfer
- Lithium
- Lithium-Ionen-Akku
- Magnesium
- Mangan
- Molybdän
- Natrium
- Neon
- Nickel
- Oganesson
- Osmium
- Oxidationszahlen
- Palladium
- Phospholipide
- Phosphor
- Plutonium
- Polonium
- PSE
- PSE: Top-Elemente
- PSE Merksätze
- Quecksilber
- Radium
- Radon
- Rhenium
- Rhodium
- Rubidium
- Ruthenium
- Sauerstoff
- Scandium
- Schwefel
- Selen
- Silizium
- Stickstoff
- Strontium
- Terbium
- Thallium
- Thorium
- Thulium
- Unedle Metalle
- Titan
- Uran
- Wasserstoff
- Wolfram
- Xenon
- Yttrium
- Zink
- Zinn